Νέα επιστημονικά δεδομένα για την αποτελεσματικότητα του ερευνητικού φαρμάκου Venetoclax

Νέα επιστημονικά δεδομένα για την αποτελεσματικότητα του ερευνητικού φαρμάκου Venetoclax σε ασθενείς με υποτροπιάζουσα/ανθεκτική χρόνια λεμφοκυτταρική λευχαιμία με έλλειψη στο χρωμόσωμα 17p
Η βιοφαρμακευτική εταιρεία AbbVie ανακοίνωσε πρόσφατα ότι μια κλινική δοκιμή φάσης 2 για το ερευνητικό της φάρμακο venetoclax πέτυχε το κύριο καταληκτικό σημείο της επίτευξης συνολικών ποσοστών ανταπόκρισης σε ασθενείς με χρόνια λεμφοκυτταρική λευχαιμία (ΧΛΛ) με έλλειψη στο χρωμόσωμα 17p, είτε στην υποτροπιάζουσα/ανθεκτική μορφή, είτε ως πρώτης γραμμής θεραπεία, σύμφωνα με ανεξάρτητη ανάλυση. Η ανοικτού σχεδιασμού μελέτη αξιολόγησε την αποτελεσματικότητα και την ασφάλεια του venetoclax, ενός αναστολέα της πρωτεΐνης BCL-2 (B-cell lymphoma-2) που αναπτύσσεται σε συνεργασία με την Genentech και τη Roche.
Τα δεδομένα από την κλινική μελέτη θα παρουσιαστούν σε επερχόμενα ιατρικά συνέδρια και θα χρησιμοποιηθούν ως πρωταρχικά στοιχεία αναφοράς για τις αιτήσεις αδειοδότησης προς τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ, τον Ευρωπαϊκό Οργανισμό Φαρμάκων και άλλες Αρχές, στις οποίες αναμένεται να καταθέσει η AbbVie πριν το τέλος του έτους. Το προφίλ ασφαλείας ήταν παρόμοιο με προηγούμενες μελέτες και δε σημειώθηκαν μη αναμενόμενες παρενέργειες για το φάρμακο.
«Τα αποτελέσματα της μελέτης αυτής καταδεικνύουν την κλινική δράση του venetoclax σε ασθενείς με υποτροπιάζουσα/ανθεκτική ΧΛΛ που παρουσιάζουν έλλειψη 17p, έναν πληθυσμό ασθενών όπου η θεραπεία ήταν ανέκαθεν δύσκολη», ανέφερε Ο Michael Severino, M.D., Αντιπρόεδρος Έρευνας και Ανάπτυξης της AbbVie. «Με βάση αυτά τα δεδομένα, σκοπεύουμε να προχωρήσουμε τις αιτήσεις για αδειοδότηση του venetoclax, διατηρώντας τη δέσμευσή μας για την περαιτέρω ανάπτυξη αυτού του ερευνητικού σκευάσματος, καθώς και άλλων από τη φαρέτρα των υπό ανάπτυξη μορίων της εταιρείας μας. Στόχος μας είναι να αναπτύσσουμε πάντα νέες θεραπευτικές επιλογές για ανθρώπους που έχουν προσβληθεί από τον καρκίνο.»
Το 2015, το venetoclax προκρίθηκε για τη διαδικασία ταχείας αξιολόγησης (Breakthrough Therapy Designation) του Οργανισμού Τροφίμων και Φαρμάκων των ΗΠΑ για την αντιμετώπιση της ΧΛΛ σε ασθενείς με έλλειψη τμήματος του χρωμοσώματος 17p και οι οποίοι έχουν λάβει προηγούμενη θεραπεία (υποτροπιάζουσα/ανθεκτική μορφή).
Σχετικά με την Χρόνια Λεμφοκυτταρική Λευχαιμία (ΧΛΛ) και την έλλειψη 17p
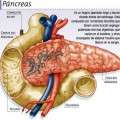
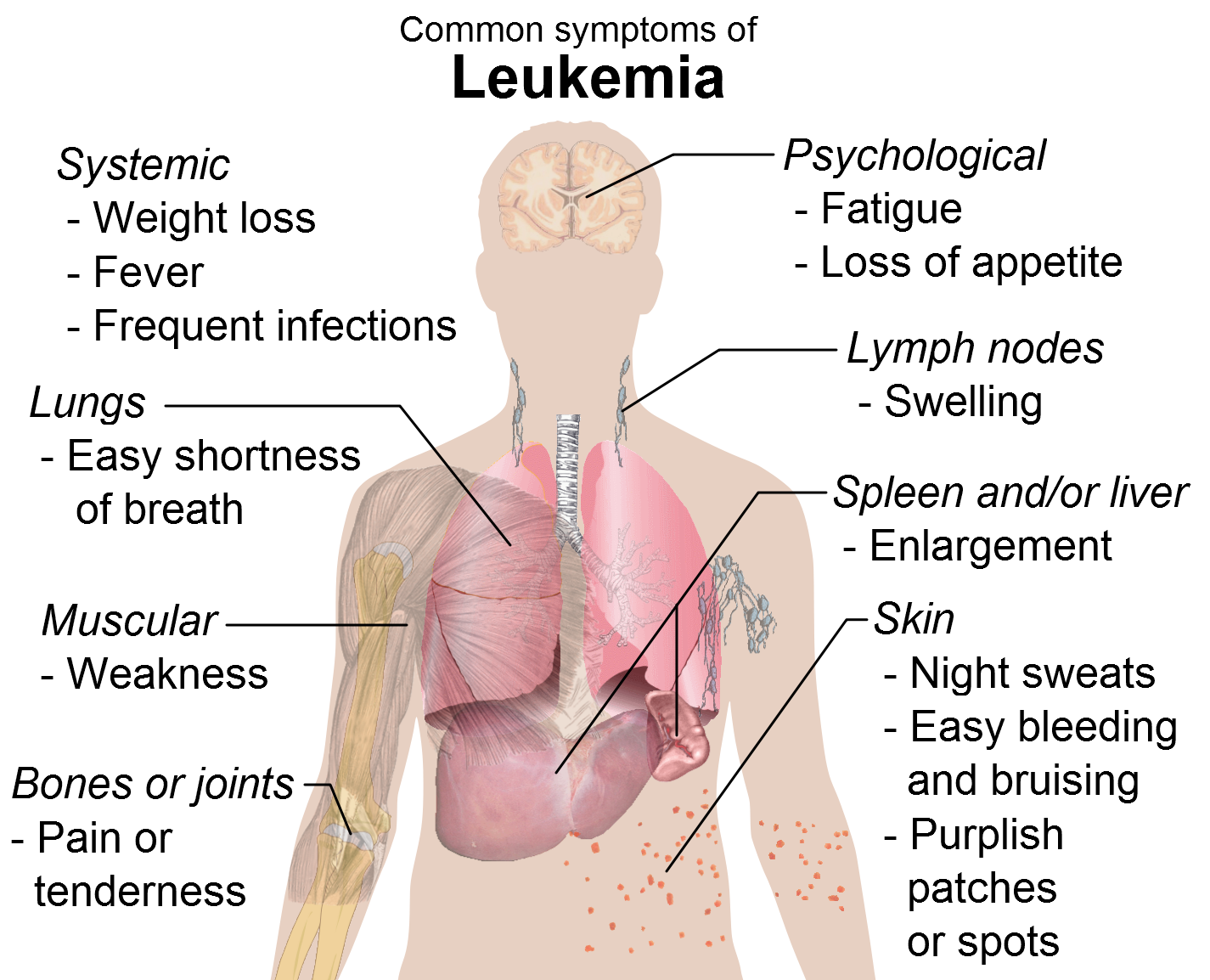
Η ΧΛΛ είναι μία βραδείας εξέλιξης κακοήθης νεοπλασία του μυελού των οστών και του αίματος, στην οποία ο μυελός των οστών παράγει υπερβολικά πολλά λεμφοκύτταρα, ένα είδος λευκών αιμοσφαιρίων1. Πρόκειται για τη συχνότερη μορφή λευχαιμίας που διαγιγνώσκεται σε ενήλικες στο Δυτικό κόσμο2. Στις Ηνωμένες Πολιτείες, η ΧΛΛ ευθύνεται για περίπου 14.620 νέες περιπτώσεις λευχαιμίας ετησίως3. Έλλειψη στο χρωμόσωμα 17p παρουσιάζει το 3-10% περίπου των ασθενών με ΧΛΛ κατά τη διάγνωση, και το 30-50% των ασθενών με υποτροπιάζουσα/ανθεκτική ΧΛΛ4. Η έλλειψη του 17p είναι μια γονιδιωματική αλλοίωση, όπου ένα τμήμα του χρωμοσώματος 17 απουσιάζει5. Ο διάμεσος χρόνος προσδόκιμου επιβίωσης για τους ασθενείς με ΧΛΛ με έλλειψη 17p είναι λιγότερο από 2-3 έτη6.
Σχετικά με τη Μελέτη Φάσης 2
Η πολυκεντρική, διεθνής, ανοικτού σχεδιασμού μελέτη φάσης 2 σχεδιάστηκε για την αξιολόγηση της αποτελεσματικότητας και της ασφάλειας του venetoclax σε ασθενείς με ΧΛΛ με έλλειψη του 17p που είτε παρουσίασαν υποτροπή είτε ανέπτυξαν αντοχή στις υφιστάμενες θεραπείες ή δεν είχαν λάβει στο παρελθόν θεραπεία για τη νόσο. Στη μελέτη εντάχθηκαν 157 ασθενείς: 107 ασθενείς στην κοορτή της κύριας μελέτης για την αξιολόγηση της αποτελεσματικότητας και 50 ασθενείς στην κοορτή επέκτασης ασφάλειας. Το κύριο καταληκτικό σημείο αποτελεσματικότητας είναι το συνολικό ποσοστό ανταπόκρισης και τα κύρια καταληκτικά σημεία ασφάλειας είναι ο αριθμός και το ποσοστό των ασθενών που παρουσίασαν ανεπιθύμητες ενέργειες σχετιζόμενες με τη θεραπεία, αλλαγές στα ευρήματα της κλινικής εξέτασης, συμπεριλαμβανομένων των ζωτικών σημείων, αλλαγές στα αποτελέσματα των κλινικών εργαστηριακών εξετάσεων και αλλαγές στα ευρήματα της καρδιολογικής αξιολόγησης. Στις δευτερεύουσες παραμέτρους αποτελεσματικότητας περιλαμβάνονται, μεταξύ άλλων, το ποσοστό πλήρους ύφεσης, το ποσοστό μερικής ύφεσης, η διάρκεια της ανταπόκρισης, η συνολική επιβίωση και η επιβίωση χωρίς εξέλιξη της νόσου.
Σχετικά με το Venetoclax
Το venetoclax είναι ένας από του στόματος ερευνητικός αναστολέας της πρωτεΐνης BCL-2 που μελετάται για τη θεραπεία ασθενών με διάφορα είδη κακοήθων νεοπλασιών. Η πρωτεΐνη BCL-2 αποτρέπει την απόπτωση ορισμένων κυττάρων, συμπεριλαμβανομένων των λεμφοκυττάρων, και μπορεί να εκφράζεται σε ορισμένα κακοήθη νεοπλασματικά κύτταρα. Το venetoclax είναι σχεδιασμένο να αναστέλλει επιλεκτικά τη λειτουργία της πρωτεΐνης BCL-2.
Το venetoclax αναπτύσσεται σε συνεργασία με την Genentech και τη Roche. Οι εταιρείες έχουν αφοσιωθεί από κοινού στην έρευνα της BCL-2 με το venetoclax, το οποίο αξιολογείται επί του παρόντος σε κλινικές δοκιμές φάσης 3 για τη θεραπεία της υποτροπιάζουσας/ανθεκτικής ΧΛΛ, μαζί με μελέτες για πολλές άλλες μορφές καρκίνου.
Το venetoclax είναι ερευνητικό μόριο/σκεύασμα και η ασφάλεια και η αποτελεσματικότητά του δεν έχουν αξιολογηθεί από τον Ευρωπαϊκό Οργανισμό Φαρμάκων (EMA), από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) ή από άλλη υγειονομική αρχή.
Σχετικά με το τμήμα Ογκολογίας της AbbVie
Η έρευνα της AbbVie στον τομέα της ογκολογίας εστιάζει στην ανακάλυψη και στην ανάπτυξη στοχευμένων θεραπειών που δρουν ενάντια στις διεργασίες στις οποίες βασίζεται ο καρκίνος για την επιβίωσή του. Η AbbVie, επενδύοντας σε νέες τεχνολογίες και προσεγγίσεις, ανοίγει νέους ορίζοντες σε ορισμένες από τις πιο διαδεδομένες και δυσίατες μορφές κακοήθων νεοπλασιών, συμπεριλαμβανομένων του πολύμορφου γλοιοβλαστώματος, του πολλαπλού μυελώματος και της ΧΛΛ. Η φαρέτρα των υπό ανάπτυξη προϊόντων της AbbVie στον τομέα της ογκολογίας περιλαμβάνει πολλά νέα μόρια, τα οποία μελετώνται στο πλαίσιο κλινικών μελετών για πάνω από 15 διαφορετικές μορφές καρκίνου και τύπους όγκων.
Σχετικά με την AbbVie
Η AbbVie είναι μία παγκόσμια βιοφαρμακευτική εταιρεία, η οποία δημιουργήθηκε το 2013 μετά από το διαχωρισμό της από την Abbott Laboratories. Αποστολή της εταιρείας είναι να αξιοποιήσει την εμπειρία της, τους αφοσιωμένους ανθρώπους της και τη μοναδική προσέγγισή της για καινοτομία, με σκοπό την ανάπτυξη προηγμένων θεραπειών που θα καλύπτουν μερικές από τις πιο σύνθετες και σοβαρές ασθένειες του κόσμου. Μετά και την εξαγορά της Pharmacyclics, η AbbVie σε παγκόσμιο επίπεδο απασχολεί πλέον περίπου 28.000 εργαζομένους (110 εκ των οποίων στην Ελλάδα) και δραστηριοποιείται σε περισσότερες από 170 χώρες.
Παραπομπές:
1 American Cancer Society (2013) “Leukemia – Chronic Lymphocytic.”
http://www.cancer.org/acs/groups/cid/documents/webcontent/003111-pdf.pdf.
2 Eichhorst, B. et al. “Chronic Lymphocytic Leukemia: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up.” Annals of Oncology 22 (Supplement 6): vi50-vi54, 2011
3 American Cancer Society (2015) “Leukemia – Chronic Lymphocytic (CLL) Topics.”
http://www.cancer.org/cancer/leukemia-chroniclymphocyticcll/detailedguide/leukemia-chronic-lymphocytic-keystatistics
4 Schnaiter, A. et al. (2013) “17p Deletion in Chronic Lymphocytic Leukemia: Risk Stratification and Therapeutic Approach.” Hematol Oncol Clin N Am 27 (2013) 289–301
5 Selner, L. et al. (2013) “What Do We Do with Chronic Lymphocytic Leukemia with 17p Deletion?” Curr Hematol Malig Rep. 8(1):81-90.
6 Stilgenbaur, S, and Zenz, T, (2010) “Understanding and Managing Ultra High-Risk Chronic Lymphocytic Leukemia.” ASH Education Book. 2010(1):481-488.